Trabajo ganador de los premios a la Investigación Científica 2022. Presentado por el Dr. Alejandro Ruiz Patiño quien agradeció inicialmente a la Academia Nacional de Medicina y a la Universidad El Bosque, como promotora en la realización de estudios en pro del entendimiento y la salud en el tratamiento del cáncer.
El cáncer de pulmón en estadio metastásico, -que es cuando más frecuentemente se identifica-, ha sido un evento de salud pública bastante llamativo. Lo que demuestran los estudios de cohortes, estudios clínicos y estudios de seguimiento llevados a cabo por diferentes entidades a nivel mundial, es que el panorama para el diagnóstico en temas de supervivencia para estos pacientes es bastante lúgubre.
Un estudio publicado en el New England Journal of Medicine en 2002, que hizo seguimiento a diferentes tratamientos, determinó que el tratamiento convencional con quimioterapia citotóxica, resultaba para ese momento en una supervivencia global de alrededor de 6 meses para el 50%, es decir, el 50% de los pacientes con un diagnóstico de adenocarcinoma de pulmón iba a fallecer a los seis meses del diagnóstico. Esto considerando el mejor escenario de estudios clínicos, donde los pacientes son seguidos más rigurosamente. En los pacientes que eran tratados en un ambiente menos controlado que el de estudios clínicos, la media de supervivencia pasaba de 6 a 4 meses, a pesar de que se ofrecían los tratamientos, ese entorno no permitía que se lograran unos resultados clínicos muy favorables.
Hacia 2020, un grupo de Epidemiología de varias instituciones, toma una base de datos poblacional en Estados Unidos conocida como SEER (Programa estadounidense de Vigilancia, Epidemiología y Resultados Finales) del Instituto Nacional del Cáncer (NCI), la principal fuente de estadísticas de cáncer en los Estados Unidos, allí se reportan la mayoría de pacientes, diagnósticos, desenlaces, tratamientos e incluso costos, de pacientes con diferentes tumores tratados en Estados Unidos. Lo que este grupo pudo notar es que desde el 2001 la incidencia ha venido aumentando, a pesar de que Organismos Internacionales, entidades de Salud Pública y hasta gobiernos han librado una batalla contra el consumo de tabaco. Si bien, los diagnósticos en fumadores han disminuido, hay un incremento en pacientes jóvenes, que no habían fumado.
Aunque la incidencia viene aumentando, paralelamente la mortalidad disminuye. Si el diagnóstico se hace tempranamente, la posibilidad de curación aumenta, pero aún se observan datos de diagnósticos tardíos y más del 60% de pacientes van a ser diagnosticados con un carcinoma de pulmón de células no pequeñas en estadio metastásico.
Los investigadores se dieron cuenta que para 2013, hubo un cambio en esa pendiente de mortalidad, empieza a caer, pasa de -1.9% entre 2001-2008 a -3.1% en 2013. Los pacientes con expectativas de vida entre 4 a 6 meses, con un diagnóstico de adenocarcinoma de pulmón, vivían más ¿pero porqué?
Desde hace tiempo se sabe que los mecanismos “involucrados” en el desarrollo del cáncer, son unas vías de señalización increíblemente complejas. Células como los neumocitos tipo I y II y otras, se diferencian y forman un tumor con base en unos perfiles propios de la célula. Esto hace que se dé una activación de unos mecanismos que estaban generalmente relacionados con el periodo embrionario, adicionalmente se perdían los mecanismos de regulación que frenaban esa conversión de esas células en tumores. Los estudios advirtieron también, que en una molécula llamada EGFR (Receptor del factor de crecimiento epidérmico), el 40-60% de los carcinomas de pulmón tenían una representación de este receptor incrementada a nivel de la membrana celular.
Igual que en tumores como el carcinoma de seno con el HER2 o el ERBB2, la posibilidad de que estos tumores sobreexpresaran esta proteína, permitió abrir una ventana terapéutica para el tratamiento de estos pacientes. Una célula nunca actúa por sí sola, tienen interacciones con sus vecinos y esa interacción se da a través de factores de crecimiento, hormonas u otros estímulos tróficos. El factor de crecimiento epidérmico está presente en esas células epidérmicas y favorece su crecimiento y diferenciación. Esto es un proceso normal que experimentamos todos los días a nivel del tracto gastrointestinal, a nivel de la piel y otros epitelios, pero este mecanismo tiene que ser regulado por esos factores de crecimiento.
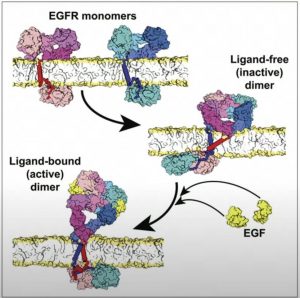
Dos moléculas o monómeros constituyen ese receptor, se une el ligando, es decir el factor de crecimiento, y al unirse se da un fenómeno de transducción de señal que es el mecanismo por el cual la célula activa una respuesta para crecer y diferenciarse.
Bajo este orden de ideas, si tenemos fenómenos que repercutan en la ganancia de función, en la activación anómala, perpetua, continua y permanente de este receptor, la célula permanecerá constantemente engañada para continuar en su ciclo de reproducción, crecimiento y desdiferenciación para llevar al desarrollo como tal de la enfermedad.
Iniciando este siglo, surgió el Getifinib, un medicamento cuyo objetivo era inhibir el dominio de la proteína que se encarga de convertir esa señal del factor trófico y convertirlo en una señal que la célula pueda entender para llevar sus procesos biológicos. La idea era bloquear esa activación cadena abajo dentro del mismo receptor y evitar que la célula siguiera replicándose, tratando de cierta forma la causa molecular de la enfermedad, pero los estudios fueron fallidos. Haciendo subanálisis, se dieron cuenta que ese beneficio terapéutico se daba en un grupo de pacientes caracterizados como mujeres jóvenes, asiáticas, no fumadoras. Con quimioterapia en estos pacientes se pasó a una media de supervivencia de 5.5 a 9.5 meses. ¿Qué tenían estas pacientes con estas características clínicas que el resto de pacientes no tenían?
La respuesta vino de un grupo de Harvard que tomó muestras de pacientes respondedores y con la técnica de secuenciación de Sanger (proceso biológico de la replicación del ADN), hizo seguimiento a esos pacientes que estaban respondiendo desde el punto de vista genómico para establecer que sucedía con estos individuos que sí respondían vs. los que no respondían. La cohorte inicial de pacientes permitió hacer una caracterización de las mutaciones que demostraban que, en el receptor de factor de crecimiento epidérmico, existían unos dominios -unas partes funcionales- que acumulaban mutaciones que engañaban a la célula para activar estas vías de transcripción. En conclusión, estos medicamentos servían a pacientes que fueran portadores a nivel del tumor de dichas mutaciones. Estas mutaciones empiezan a conocerse como mutaciones sensibilizantes a inhibidores de tirosina quinasa.
El tratamiento con inhibidores de tirosina quinasa en EGFR, cambia el panorama pasando de 4-6 meses a 38.6 meses como media de supervivencia. El tratamiento en primera línea con Osimertinib, cambia drásticamente el curso de la enfermedad, pero si bien, el beneficio es drástico en la media de supervivencia existen unos pacientes que a pesar de que reciben el tratamiento, presentan un deterioro clínico y una progresión muy rápida.
El grupo de investigadores ganadores de FICMAC, plantearon un diseño de estudio para poder establecer cuáles eran esas medidas pronósticas. ¿Qué pacientes iban a tener una buena respuesta a este tratamiento y cuáles no? Se seleccionaron 2 cohortes de pacientes. La primera o cohorte A, pacientes que presentaban una progresión de la enfermedad, dentro de los tres meses posteriores al inicio del tratamiento con Osimertinib y se comparaba con pacientes respondedores o cohorte B, es decir, que tienen una supervivencia libre de progresión de enfermedad o muerte, más allá de los 18 meses. Se pretendía hacer una caracterización genómica tanto del tejido como una biopsia líquida, más una cuantificación de otros factores que pudieran determinar qué pacientes cuentan o no cuentan con una resistencia intrínseca al tratamiento con Osimertinib. Hacia la semana 8 se debía hacer la toma de una muestra que permitiera la detección del EGFR, a nivel de sangre periférica -biopsia líquida-, en búsqueda de material genético u otros componentes celulares, siendo una representación del tumor.
Los tumores crecen y al crecer tienen unos procesos donde las células entran en apoptosis -muerte celular-, una cantidad de ese material genómico y otro tipo proteómico y transcriptómico, sale al torrente sanguíneo, tiene una vida media corta pero rastreable. Esto permite hacer un seguimiento molecular activo de la enfermedad. Si el paciente es tratado y no cuenta con ADN circulante posterior al tratamiento, se podría asumir que la enfermedad se encuentra controlada, esa es la idea de la biopsia líquida en seguimiento.
Los resultados incluyeron un total de 32 pacientes, se analizaron factores como el sexo, el historial de tabaquismo, su capacidad funcional, número de sitios metastásicos, las mutaciones, el EGFR. Dependiendo del tipo de mutación, puede variar la respuesta. Por ejemplo, ubicar una mutación T790M que es uno de los mecanismos de resistencia que desarrollan las células y las hacen resistentes a los tratamientos de primera línea como el Getifinib.

Los hallazgos frente a los perfiles genómicos de la cohorte A y B, muestran un listado de genes altamente relevantes para todos los procesos moleculares frente a las diferentes variaciones del EGFR (en la parte superior). Cada perfil molecular cambia completamente el comportamiento y el pronóstico de esta enfermedad. Los investigadores notaron que el perfil mutacional de los refractarios o resistentes era bastante diverso pero que caía en unas vías de señalización que son muy conocidas en cáncer y que se conocen como responsables de esa resistencia a este y otros fármacos Incluso en otras patologías.
Otros hallazgos
El TP53, que es uno de los genes más importantes en la preservación de la integridad celular, se encontraba alterado en una gran proporción de pacientes. Y aparecen otros genes alterados como el RB1, que controla la forma en que las células crecen y se dividen, PI3K, vía de señalización de la fosfatidilinositol- 3-kinasa, crucial en numerosos aspectos del crecimiento y la supervivencia celular, NF1, MET, KRAS, EGFR, y otras variantes adicionales de resistencia. Si bien, el perfil molecular es diverso también es caracterizable, y esto permite conocer cómo es esta enfermedad y cuál es la consecuencia.
Se habla de mutaciones puntuales, pero también de amplificación. Los tumores tienen una mutación que los guía -mutaciones conductoras o mutaciones drivers-, pero ganan mutaciones en otros genes que tienen unos principios similares, pero son ajenos al EGFR, es decir, son enfermedades que están mutando en otros geno y fenotipos totalmente distintos a los vistos.
En los marcadores AXL y BIM, presentes en los procesos de apoptosis y respuestas celular mitocondria, se presentan dos situaciones. Los pacientes que estaban logrando una respuesta a largo plazo, tienen una disminución en AXL. Si hay un gen que favorece la apoptosis, bajos niveles de ese gen van a ser efectivos porque la célula será capaz de entrar en ese proceso, pero si hay una célula resistente a ese mecanismo, la compensación celular será elevar esos mecanismos proapoptóticos (que propician la apoptosis y estorba la aparición y progresión del cáncer) y ese es el fenómeno que se observa con AXL. En el caso de BIM ocurre lo contrario, los supervivientes por largo tiempo presentan niveles altos en BIM y esto pasa porque BIM actúa a nivel del Bcl-2, también conocido en neoplasias hematológicas que tiene que ver con las vías de apoptosis y resistencia a la misma. Los pacientes primariamente resistentes expresan poco BIM, poca capacidad de la célula de entrar en apoptosis, confirmando los hallazgos del AXL
La determinación de cfDNA – ADN libre circulante- en biopsia líquida mostró que los pacientes que negativizaban ese valor o esa prueba tenían una mejor supervivencia.
En TMB score -carga mutacional tumoral- que agrupa las mutaciones a lo largo del genoma del tumor en un solo parámetro, se encontró que si el TMB se encuentra alto es un tumor mutante y por consiguiente pobre respondedor, si el tumor tiene cargas mutacionales bajas, favorecerá una mejor respuesta.
Si se tienen en cuenta los perfiles hiperpermutados vs. los no hipermutados se observa que a pesar de la existencia de un mecanismo “driver” o conductor, que en este caso son las mutaciones sensibilizantes del EGFR, todo ese genoma o esos perfiles adicionales confieren la divergencia en las respuestas clínicas al tratamiento con Osimertinib.
 En la imagen, las curvas de supervivencia reflejan que ≤2 conmutaciones vs. ≥ 3 conmutaciones, el cambio es drástico en tiempo de supervivencia. Uno de los grandes beneficios para el tratamiento del cáncer y otras enfermedades es que permite evaluar cuál va a ser el comportamiento de la enfermedad a largo plazo y así mismo ofrecer un tratamiento, en este caso en la supervivencia libre de progresión (PFS-Progression Free Survival) y la supervivencia global (OS- Overall Survival).
En la imagen, las curvas de supervivencia reflejan que ≤2 conmutaciones vs. ≥ 3 conmutaciones, el cambio es drástico en tiempo de supervivencia. Uno de los grandes beneficios para el tratamiento del cáncer y otras enfermedades es que permite evaluar cuál va a ser el comportamiento de la enfermedad a largo plazo y así mismo ofrecer un tratamiento, en este caso en la supervivencia libre de progresión (PFS-Progression Free Survival) y la supervivencia global (OS- Overall Survival).
El perfilamiento genético se hacía con la expectativa de que el genoma fuera estable en el individuo pero evidentemente no ocurre así y el testeo secuencial permite conocer el comportamiento de la enfermedad, hacer modificaciones al tratamiento, intensificarlo, dar otras alternativas y seguir en el camino de incrementar la supervivencia en los pacientes como ha ocurrido los últimos 20 años.
Autor principal: Diego Fernando Chamorro Ortiz
Coautores: July Rodríguez, Alejandro Ruiz-Patiño, Darwin A. Moreno-Pérez, Dora V. Ardila, Lucia Viola, Camila Ordóñez-Reyes, Carolina Sotelo, Sergio Mejía, Elvira Jaller, Carlos Vargas, Hernán Carranza, Jorge Otero, Pilar Archila, Maritza Bermúdez, Tatiana Gámez, Juan Esteban García, Andrés F. Cardona.
Entidad: FICMAC- Fundación para la Investigación Clínica y Molecular Aplicada al Cáncer.
Resumen de la intervención, Victoria Rodríguez G., responsable de plataformas digitales en la ANM.
Visitas: 59