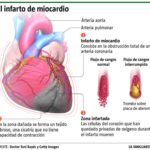
La falla cardiaca es la primera causa de mortalidad en las enfermedades del corazón.Normalmente el corazón se compone de un 70% de matriz extracelular (MEC) y un 30% de cardiomiocitos; en el corazón isquémico existen alteraciones en esta matriz. Publicaciones recientes han puesto de relieve el potencial de esta matriz sembrada con células de médula ósea (CMO), para promover los efectos paracrinos en los tejidos isquémicos (por ejemplo, la secreción de factores angiogénicos), y sugieren que la señalizaciones paracrinas, en lugar de incorporación celular, promueven la recuperación funcional.
OBJETIVO: Evidenciar en modelos teóricos, los posibles mecanismos de compensación celular e interacción con la matriz extracelular biológica en forma de transplante e implante, como tratamiento en pacientes infartados con falla cardiaca avanzada.
Existen diferente componentes tisulares asociados en el proceso de reparación y remodelación cardiaca. Se ha demostrado que varias metaloproteinasas -MMP (incluyendo MMP-1, 3, 7, 9, 13 y 14) procesan proteolíticamente varios factores derivados de fibroblastos, incluyendo el Factor de crecimiento transformante (TGFα y TGFβ) y el factor de crecimiento de tejido conectivo (CTGF) a su vez también pueden estimular la síntesis de MMP-1, 2, 3, 9, 12 y 14, para disminuir los niveles de los inhibidores de las enzimas de metaloproteinasas (TIMP-1 y TIMP-2), y afectar la quimio atracción y la adhesión de los fibroblastos en la matriz extracelular del miocardio, el CTGF también es inducido por el factor de necrosis tumoral alfa (TNFα) que es miembro de un grupo de otras citocinas que estimulan la fase aguda de la reacción inflamatoria, así mismo aumenta las MMP y disminuye los TIMP en fibroblastos o células endoteliales vasculares.
Es importante destacar que la cicatriz del infarto es dinámica y está compuesta de componentes celulares que forman un tejido metabólicamente activo y vascularizado. En la zona infartada, la Matriz extracelular es modificada, el colágeno tipo I disminuye entre el 80 al 40% y el colágeno tipo III aumenta del 10 al 35%, creando una fibrosis patológica. El resultado es un remodelado ventricular adverso, dilatación y disfunción tanto diastólica como sistólica. El adelgazamiento de la pared del infarto amplifica el aumento del estrés de la pared, lo que afecta en mayor medida la función del ventrículo izquierdo. Es necesario recordar que durante la fase de curación, el tejido del infarto se repara y se remodela a través de la degradación y síntesis de la matriz extracelular, la angiogénesis, la apoptosis y la proliferación celular que se combina de manera temporalmente regulada.
RESULTADOS:
1-El trasplante de células para la regeneración del miocardio isquémico está limitado por la escasa viabilidad del injerto y la retención celular baja, debido a que el 73% de las células transplantados sufren apoptosis por procesos de adaptación infructuosos aumentando el porcentaje de colágeno tipo III del ecosistema celular, vinculado con las vías moleculares de las 16 proteínas analizadas.
2- El uso de una matriz celular de colágeno favorece la retención de células intra-miocárdicas y crea un microambiente que promueve la supervivencia celular, al trasplantar matriz con células pluripotentes (células- Matriz) logran crear un ambiente sostenible, el cual disminuye la fibrosis patológica del infarto agudo de miocardio, que luego se ve afectada por las proteínas VEGF, FGF- 1, FGF- 2.
3- Los estudios de investigación sobre terapia celular en infarto, han demostrado una notable mejoría de los síntomas en pacientes evaluados. Sin embargo, no se logró demostrar ningún beneficio en la reducción de las tasas de mortalidad. Durante el análisis de proteínas inductoras de apoptosis celular, se esclareció que el problema es por la falta de la inducción de procesos angiogénicos en el transplante y migración celular.
CONCLUSIONES:
1-El trasplante de células para la regeneración del miocardio isquémico está limitado por la escasa viabilidad del injerto y la retención celular baja.
2-El uso de una matriz celular de colágeno favorece la retención de células intramiocárdica y crea un microambiente que promueve la supervivencia celular.
3- La terapia celular ha demostrado en diversos trabajos la mejora de los síntomas, pero no se demostró ningún beneficio en la mortalidad.
No se ha encontrado respuesta y viabilidad en los estudios donde involucren experimentos con estas moléculas, receptores, genes, proteínas y factores para recuperar el corazón pos infarto.
Fibrosis: Ruta molecular que permite proliferación y control al estrés celular pos infarto. El mayor problema es que las células cardiacas, no se regeneran, así que el órgano pierde capacidad de bombeo deforma permanente.El órgano se va debilitando de manera progresiva y permite el desarrollo de células que no se contraen, y por eso se pone en riesgo la supervivencia de las personas que han sufrido un infarto severo.
Referencias
Chachques JC. Myocardial Assistance by Grafting a New Bioartificial Upgraded Myocardium (MAGNUM Trial): Clinical Feasibility Study. Soc Thorac Surg. Volume 85(Issue 3):Pages 901–8.
Gerd P Meyer, Kai C, Wollert, JL, Jan Steffens PL. Intracoronary Bone Marrow Cell Transfer After Myocardial Infarction Eighteen Months’ Follow-Up Data From the Randomized, Controlled BOOST (BOne marrOw transfer to enhance ST-elevation infarct regeneration) Trial. Circulation. 2006;113(1):1287–94.
Lovell-Badge R. The future for stem cell research. Nature. 2001;414(1):88–91.
Alvarez-Dolado M, Pardal R, Garcia-Verdugo JM, Fike JR, Lee HO, Pfeffer K et al. Fusion of bone-marrow-derived cells with Purkinje neurons, cardiomyocytes and hepatocytes. Nature. 2003;425(1):968–73.
Tara L. Rasmussen. Getting to the Heart of Myocardial Stem Cells and Cell Therapy. Circulation. 2011;123(1):1771–9.
Fibrosis
Autores:
Luisa Fernanda Zúñiga-Cerón 1, Jhan Sebastián Saavedra-Torres2, Guillermo Wilson Muñoz Ordoñez3, Nelson Adolfo López Garzón4, María Virginia Pinzón Fernández 5, Carolina Salguero6, Jheymmy Lorena Garcés Gómez7. EVIDENCIA DE INTERACCIÓN Y FUNCIÓN DE PROTEÍNAS VINCULADAS EN EL TRANSPLANTE CELULAR Y DE MATRIZ EXTRACELULAR EN EL INFARTO AGUDO DE MIOCARDIO.
1-2. Estudiantes del programa de Medicina, Facultad de Medicina, Universidad Nacional de Colombia. Grupo de Investigación en Salud (GIS)- Universidad del Cauca- Popayán / Bogotá, Colombia.
3.Esp. Cirugía general; Sub Esp. Cirugía vascular. Profesor Asociado, Departamento de Cirugía General, Facultad de Ciencias de la Salud, Universidad del Cauca.
4. MD Internista – Cardiólogo nuclear y Ecocardiólogo. Msc en Educación, Candidato a PhD de Educación, Profesor Asociado de la Universidad del Cauca.
5. Bacterióloga, Esp. Educación, MSc. Salud pública, PhD. Antropología, Profesora Titular de la Universidad del Cauca.
6. PhD. Departamento de Biología Celular y Molecular, Universidad de Harvard, Cambridge, Massachusetts 02138, USA. Grupo de Investigación en Salud (GIS).
7. Escuela Latinoamérica de Medicina Cuba, Universidad de Ciencias Médicas de las Tunas, La Habana, Cuba, Grupo de Investigación en Salud (GIS).
Visitas: 25