La obesidad y el sobrepeso se definen por la organización mundial de la Salud (OMS), como la acumulación anormal o excesiva de grasa, que puede ser perjudicial para la salud; el indicador más utilizado es el IMC y está dado por el peso en kilogramos dividido por el cuadrado de la talla en metros (kg/m2); el valor para indicar sobrepeso es igual o superior a 25 y obesidad igual o superior a 30.
Cualquiera que sea la causa para que se presente situación de obesidad en una persona, es importante lograr entender los mecanismos asociados con la regulación del equilibrio energético porque son vitales para analizar y correlacionar la fisiopatología, etiología y patología. Esta situación pandémica que registra la organización mundial de la Salud (OMS), de acuerdo con los últimosregistros, para este año se reporta que en el mundo mueren aproximadamente 2,8 millones de personas por sobrepeso y obesidad; entendiéndose este como un problema que prevalece en países de ingresos altos, medianos y bajos. Con el peso corporal se asocian dos sistemas: El neurovegetativo porque interviene en el mantenimiento y equilibrio del balance energético. El endocrino y neuroendocrino porque es evidente que en condición de obesidad hay alteraciones hormonales sin embargo el mecanismo de algunas de ellas y su asociación clínica, no han sido completamente dilucidados.
El sistema neuroendocrino: las hormonas como vehículos accesorios de la obesidad.
El aumento en los niveles de insulina y la resistencia a la misma, así como el aumento del tejido adiposo, son correlaciones atribuibles al sistema endocrino por su asociación hormonal, al igual que la disminución en la función de la hormona somatotropa a nivel del sistema hipotálamo hipófisis; se ha observado que por cada unidad que aumente el índice de masa corporal (IMC) a una determinada edad se disminuye la secreción de GH hasta en un 6%, también a nivel de neurohipófisis se disminuye la respuesta a estímulos de prolactina; algunos estudios sugieren que el aumento en la secreción de somatostatina ocurre porque se inhibe la liberación de hormona gonadotropa y aunque en algunos casos los defectos en el eje GH-IGF que se presentan en la obesidad pueden ser reversibles con la pérdida de peso inducida por dieta o por cirugía; el mecanismo que conlleva a manifestar obesidad seguramente es multifactorial, por ejemplo algunos investigadores sugieren la posibilidad que el aumento de los ácidos grasos libres contribuye con esta alteración, al igual que la disminución de la secreción de grelina.
Cuando las somatotropas, se encuentran en descanso funcional por mucho tiempo y luego se estimulen por varios estímulos, no se vuelven atróficas bajo condición de obesidad y se muestra normal la función hormonal trófica hipotalámica; probablemente la causa principal para que se vea alterada la secreción de GH en la obesidad puede ser una alteración en el hipotálamo, debida a una función hipofisaria anormal o alteración en las señales periféricas que estimulan la hipófisis o el hipotalámo.
En el sexo femenino la acumulación de tejido graso a nivel abdominal también se asocia con el aumento en la secreción de andrógenos a hiperandrogenismo y bajos niveles de proteína transportadora de hormonas sexuales; mientras tanto para el sexo masculino los niveles de testosterona y las concentraciones de gonadotropina se observan disminuidas, sobre todo en aquellos casos que correlacionan parámetros para obesidad mórbida; de otro lado también se percibe elevación en los niveles de cortisol libre en plasma, pero que no cambian con el incremento de peso.
Mientras tanto la grelina es un factor orexinergico que se observa en bajo nivel para personas obesas; en este estado también se encuentran aumentados los niveles de hormona estimulante de la tiroides (TSH) y triyodotirosina (T3) libre.
En el tejido adiposo la secreción de leptina por gramo es el doble en personas obesas, comparada con individuos de peso normal ya que la presencia de esta hormona es un indicador metabólico de suficiencia energética.
La literatura científica describe dos formas principales del péptido YY, PYY1 y PYY3 el cual se sintetiza y libera al torrente sanguíneo por células neuroendocrinas especializadas llamadas L, que se encuentran en el tracto gastrointestinal distal; este péptido aumenta como respuesta a la carga calórica, ingesta de nutrientes, , consistencia y composición del alimento.
Existen mecanismos hormonales y hormonales involucrados en la liberación inicial del péptido YY asociados con el aumento inicial posprandialal poco tiempo de ingesta antes de que los nutrientes alcancen las células L del tracto gastrointestinal distal.
En 2002, Batterham et al propusieron que la administración periférica de PYY3, disminuía la ingesta de alimentos en roedores y en humanos con peso normal y posteriormente demostraron que el efecto anoréctico del PYY3 se conservaba en personas obesas y que contribuía con la saciedad posprandial. Actualmente existen estudios que evidencian el papel del PYY3 en la regulación del peso corporal a largo plazo, aunque este péptido PYY3 es selectivo para el receptor Y2 (Y2R). Un papel importante de este receptor como mediador del efecto anoréxico del PYY3 durante la alimentación lo identificó inicialmente Batterham et al observando que los ratones sin el receptor Y2 eran resistentes a los efectos anorexígenos del PYY3
PP es un péptido producido predominantemente por las células F, localizadas en la periferia de los islotes de Langerhans del páncreas y en menor medida en el colon. Existen evidencias que sugieren que PP es importante en la regulación del peso corporal en roedores, pero aún no se sabe con claridad el papel del PP en la patogénesis de la obesidad no sindrómica.
La amilina es una hormona peptídica neuroendocrina que simultáneamente se segrega con la insulina por las cèlulas beta pancreáticas como respuesta ante la ingesta de nutrientes, a las hormonas incretinas y al impulso neural; la amilina tiene acciones glucoregulatorias que complementan las acciones de la insulina, suprimen la secreción de glucagón posprandial y retrasa el vaciado gástrico.
Algunos investigadores han discutido una disfunción neuroendocrina que produce una secreción anormal de TSH como consecuencia del aumento en las concentraciones de TSH en la obesidad, específicamente se ha observado que la lectina altera el eje hipotálamo-hipofisario; sin embargo, con el test de TRH se ha logrado descartar algún tipo de alteración en la respuesta de la hipófisis en niños obesos con niveles de TSH aumentados.
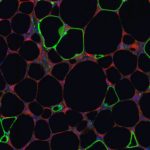
El adipocito.
El adipocito es la célula fundamental del tejido adiposo, es la encargada de almacenar el exceso de energía en forma de triglicéridos y liberarlos, en momentos de necesidad energética. El desarrollo del adipocito, se puede dar por hipertrofia o hiperplasia, se considera que éste aumenta su volumen hasta llegar a un umbral crítico que predispone, a un proceso de hiperplasia, estimulando a una célula precursora para que genere una nueva célula de adipocito. A la actualidad, se sabe que esta célula, secreta diversidad de adipoquinas, de las cuales se desconoce específicamente su función, sin embargo, se ha estudiado bien, el mecanismo de la adiponectina y la leptina, siendo protagónico en el rol de la obesidad.
Autores: Sirsa Aleida Hidalgo-Ibarra1. Laura María Bejarano-Alos2. Juan Carlos Ducuara-Hernández2. 1-Bióloga. Magíster en Ciencias Biomédicas. Docente. Facultad de Ciencias de la Salud. Programa de Medicina. Universidad Santiago de Cali. 2-Estudiantes de Medicina. Facultad de Ciencias de la Salud. Universidad Santiago de Cali – Seccional Palmira (V). Correspondencia. E-mail: laura.bejarano00@usc.edu.co
Ver Sistema neuroendocrino y su correlación con la obesidad. JCDH
Visitas: 55