El número de posibles dianas terapéuticas que hay en la superficie de las proteínas humanas es mucho mayor de lo que se creía, según un estudio del Centro de Regulación Genómica de Barcelona. Los autores han logrado trazar el primer mapa de estas dianas tan difíciles de encontrar, conocidas como sitios alostéricos.
Una nueva técnica desarrollada por un equipo científico del Centro de Regulación Genómica (CRG) de Barcelona ha revelado la existencia de multitud de ‘puertas ocultas’ que controlan la función de las proteínas y que podrían, en teoría, utilizarse como dianas para cambiar drásticamente la evolución de enfermedades tan diversas como la demencia, el cáncer y las enfermedades infecciosas.
El método, en el que se ejecutan decenas de miles de experimentos a la vez, se ha utilizado para trazar el primer mapa de estas dianas tan difíciles de encontrar, conocidas como sitios alostéricos, en dos de las proteínas humanas más habituales, lo cual ha evidenciado que son abundantes e identificables.
Esta técnica podría cambiar las reglas del juego en el descubrimiento de fármacos y dar lugar a unos medicamentos más seguros, más inteligentes y eficaces. Permite a los laboratorios de investigación de todo el mundo buscar y aprovechar las vulnerabilidades de cualquier proteína, incluidas las que hasta ahora se consideraban “dianas imposibles”, según los autores.
André Faure, investigador postdoctoral del CRG y coautor del trabajo señala que “no solo resulta que estos potenciales sitios terapéuticos son abundantes, sino que hay pruebas de que pueden manipularse de muchas formas diferentes”.
Modular la actividad como si fuera un termostato
Además, explica que “en lugar de solo activarlos y desactivarlos, podríamos modular su actividad como si fuera un termostato. Desde el punto de vista de la ingeniería, es como si hubiéramos encontrado oro, porque nos da mucho espacio para diseñar fármacos inteligentes que se dirigen a lo malo y omiten lo bueno”, apunta Faure.
Las proteínas tienen una función primordial en todos los organismos vivos y desempeñan funciones vitales como aportar estructura, acelerar las reacciones, actuar como mensajeros o combatir enfermedades. Están formadas por aminoácidos y se pliegan en innumerables formas diferentes en el espacio tridimensional. La forma de una proteína es fundamental para su función. Solo un error en una secuencia de aminoácidos puede tener consecuencias potencialmente devastadoras para la salud humana.
La alostería es uno de los grandes misterios sin resolver de la función de las proteínas. Los efectos alostéricos se producen cuando una molécula se une a la superficie de una proteína, lo cual a su vez provoca cambios en un sitio distante en la misma proteína, regulando su función por control remoto.
Muchas mutaciones patógenas, incluidos numerosos iniciadores oncogénicos, son patológicas por sus efectos alostéricos.
Pese a su importancia fundamental, los sitios alostéricos son increíblemente difíciles de encontrar, porque las normas que rigen el funcionamiento de las proteínas a nivel atómico no están a la vista.
Por ejemplo, una proteína puede cambiar de forma en presencia de una molécula nueva y dejar al descubierto bolsas profundas en su superficie que podrían ser alostéricas pero que no son identificables solo mediante la determinación de estructuras convencional.
Tradicionalmente, los ‘cazadores de fármacos’ han diseñado tratamientos que se dirigen al sitio activo de una proteína, la pequeña región donde se producen las reacciones químicas o donde se unen las dianas. El inconveniente de estos fármacos, conocidos como fármacos ortostéricos, es que los sitios activos de muchas proteínas son muy similares y los fármacos tienden a unirse e inhibir muchas proteínas diferentes a la vez, lo que puede provocar efectos secundarios.
En comparación, la especificidad de los sitios alostéricos significa que los fármacos alostéricos son unos de los medicamentos más eficaces que existen en la actualidad. Muchos fármacos alostéricos, que tratan varias afecciones que van desde el cáncer o el sida hasta trastornos hormonales, se han descubierto por casualidad.
“Experimento por fuerza bruta”
Los autores del estudio abordaron este problema desarrollando una técnica llamada PCA de doble profundidad (ddPCA), que describen como un “experimento por fuerza bruta”.
“Rompemos las cosas adrede de miles de maneras distintas para formar una imagen completa de cómo funciona algo”, indica Ben Lehner, otro de los autores.
Según Lehner. “es como si sospecharas que una bujía no funciona, pero en lugar de comprobar solo eso, el mecánico desmontara todo el coche y revisara todas las piezas una por una. Al analizar diez mil cosas a la vez, identificamos todas las piezas que son realmente importantes”, recalca.
El método funciona cambiando los aminoácidos que componen una proteína, lo que da lugar a miles de versiones diferentes de la proteína con solo una o dos diferencias en la secuencia. Entonces se analizan todos los efectos de las mutaciones al mismo tiempo en células vivas en el laboratorio.
“Cada célula es una minifábrica que crea una versión diferente de la proteína. En un solo tubo de ensayo tenemos millones de factorías diferentes y así podemos analizar muy rápidamente cómo funcionan todas las versiones diferentes de una proteína», añade el Lehner.
Los datos obtenidos en los experimentos se introducen en redes neuronales, algoritmos que analizan los datos imitando el funcionamiento del cerebro humano, y esto da lugar a unos mapas completos que determinan la ubicación de los sitios alostéricos en la superficie de las proteínas.
Una de las grandes ventajas del método es que se trata de una técnica asequible, accesible para cualquier laboratorio de investigación del mundo.
“Simplifica enormemente el proceso necesario para encontrar sitios alostéricos. La técnica trabaja con un nivel de precisión mejor que varios métodos de laboratorio diferentes más caros y lentos”, comenta Júlia Domingo, primera autora del estudio.
“Nuestra esperanza es que otros científicos utilicen la técnica para mapear de forma rápida y exhaustiva los sitios alostéricos de las proteínas humanas una a una”, dice Domingo.
Uno de los beneficios de la técnica a más largo plazo es su potencial para estudiar la función y la evolución de las proteínas.
Los investigadores opinan que, si se amplía, el método podría algún día propiciar avances que puedan predecir con precisión las propiedades de las proteínas a partir de sus secuencias de aminoácidos.
Nueva era de biología molecular predictiva
Si esto se lograra, creen que se marcaría el inicio de una nueva era de biología molecular predictiva, que permitiría un desarrollo mucho más rápido de los medicamentos nuevos y una industria limpia y basada en la biología.
“Aunque algunas herramientas pueden predecir la estructura de una proteína leyendo su secuencia, nuestro método va un paso más allá y nos dice cómo funciona una proteína. Forma parte de una visión más amplia en que la biología puede diseñarse mediante ingeniería como los aviones, los puentes o los ordenadores”, dice Lehner.
El investigador añade que “llevamos más de 70 años enfrentándonos a los mismos retos, pero resulta que son más manejables de lo que pensábamos. Si lo logramos, se abrirá la puerta a un nuevo campo con posibilidades sin precedentes”, concluye.
Lehner et al. “Mapping the energetic and allosteric landscapes of protein binding domains”. Nature (abril, 2022).
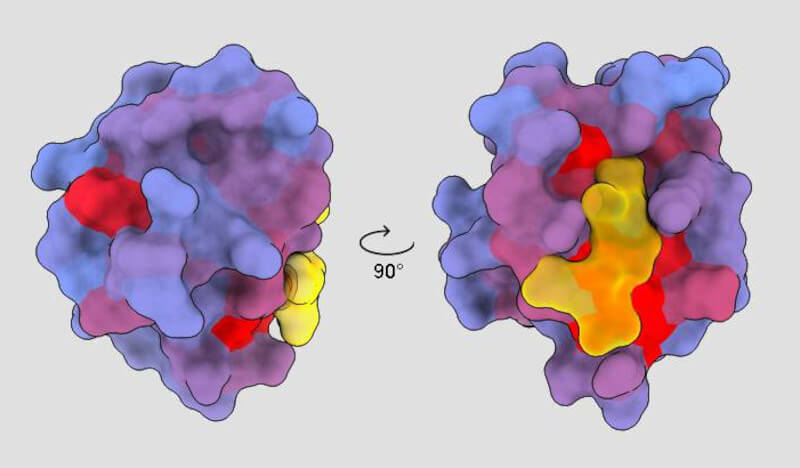
Imagen: Imagen tridimensional de la proteína humana PSD95-PDZ3 vista desde diferentes ángulos. Se muestra el compañero de unión CRIPT (amarillo) en el sitio activo con el gradiente de color azul a rojo que indica un potencial creciente de efectos alostéricos. / André Faure /CRG
Fuente: CRG
Derechos: Creative Commons.
Visitas: 5